Determinazione del numero di piatti teorici
La distillazione all'interno del separatore avviene favorendo l'evaporazione dell'ammoniaca, la quale ha una tensione di vapore più alta ma comunque confrontabile a quella dell'acqua: tale situazione rende necessario l'utilizzo di una colonna di distillazione . Supposte condizioni ideali, in ogni piatto si raggiungerà un equilibrio tra la fase vapore e la fase liquida, e i fluidi saranno saturi. Le cadute di pressione sono trascurate.
Per determinare il numero dei piatti teoricamente necessari alla distillazione della portata mR fino ad ottenere la portata mD con concentrazione ξD è necessario dividere la colonna di distillazione in una sezione di arricchimento, ove sarà sottratto il calore |qD|, ed una sezione di esaurimento dove sarà somministrato il calore qB.
Sezione di arricchimento
Con riferimento alla superficie di controllo rappresentata in figura, la quale racchiude la sezione di arricchimento, ricordando l'espressione di qD, il bilancio di massa e di energia permette di ricavare la seguente espressione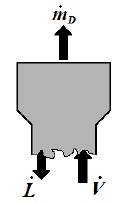
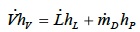
Ove
V rappresenta le condizioni del vapore saturo;
L rappresenta le condizioni liquido saturo;
P identifica il polo superiore di distillazione.
Si fa notare che all'interno del separatore non vi è solo una coppia di V ed L, poiché si identificano diverse portate, ognuna caratterizzata da una concentrazione di ammoniaca diversa e dunque stati differenza in corrispondenza della saturazione.
La relazione è valida per tutti i piatti, ed indicando con k il generico piatto questa si presenta nella forma seguente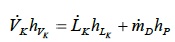
Graficamente tale espressione è rappresentabile con un segmento congiungente i punti LK,VK e P. Per il piatto più alto (1° piatto) è noto il punto P, mentre il punto L1 è ricavabile dalla condizione di equilibrio termodinamico tra il vapore saturo prodotto dalla colonna nelle condizioni D (coincidenti con le condizioni 1) e il liquido saturo nelle condizioni L1; in altre parole L1 e D giacciono sulla medesima isoterma. Il punto V1 si troverà per quanto detto sulla congiungente L1-P in corrispondenza della curva di rugiada. La portata V1 è a sua volta in equilibrio termodinamico con il liquido in condizioni L2. Tracciando l'isoterma si determina L2 e di conseguenza V2. Si itera tale procedura fino a quando la retta passante per i punti LK e P si trova a destra della retta polare. La scelta arbitraria di P conduce ad avere tre piatti teorici.
Sezione di esaurimento
Con riferimento alla superficie di controllo rappresentata in figura, la quale racchiude la sezione diimpoverimento, il bilancio di massa e di energia permette di ricavare la seguente espressione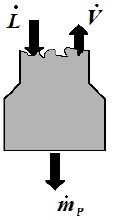
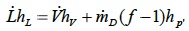
Ove P' identifica il polo inferiore di distillazione. Tale relazione è valida per ogni n-esimo piatto: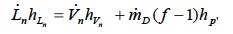
Come nel caso della sezione di arricchimento, graficamente tale espressione è rappresentabile con un segmento congiungente i punti Ln,Vn e P'. Per il piatto più basso è noto il punto P', mentre il punto VN è ricavabile dalla condizione di equilibrio termodinamico tra esso ed il liquido saturo prodotto dalla colonna nelle condizioni B (coincidenti con le condizioni 8); in altre parole VN e B giacciono sulla medesima isoterma. Il punto LN si troverà sulla congiungente VN-P' in corrispondenza della curva di bolla. La portata LN è a sua volta in equilibrio termodinamico con il vapore saturo in condizioni VN-1. Tracciando l'isoterma si determina VN-1 e di conseguenza LN-1. Si itera tale procedura fino a quando la retta passante per i punti Ln e P' si trova a sinistra della retta polare. Il procedimento porta a determinare un numero di piatti teorici pari a tre.
Si sottolinea che nella realtà la condizione di equilibrio termodinamico richiederebbe un tempo di contatto tra le fasi vapore e liquido tendenzialmente infinito. Di conseguenza il numero dei piatti teorici risulta essere un limite inferiore ai piatti realmente necessari.
Continua a leggere:
- Successivo: Analisi di secondo principio
- Precedente: Risultati
Dettagli appunto:
- Università: Politecnico di Torino
- Facoltà: Ingegneria
- Corso: Ingegneria per l'Ambiente e il Territorio
- Esame: Tecniche del freddo e criogenia
- Docente: Silvi
Altri appunti correlati:
- Ciclo a semplice compressione di vapore di un gruppo frigorifero
- Calore e termoterapia
- I cicli criogenici
- Biologia Vegetale
- Scienze Infermieristiche
Per approfondire questo argomento, consulta le Tesi:
- Realizzazione di rivestimenti intermetallici finalizzati alla protezione di componenti impiegati alle alte temperature
- Bilancio energetico ed idrologico nello strato superficiale atmosferico durante eventi monsonici
- Studio della correlazione tra raggi cosmici ed altri parametri atmosferici mediante l’utilizzo di reti neurali
- Analisi termica di leghe di magnesio ZE41A utilizzate in ambito aeronautico
- L'analisi exergetica quale metodo di ottimizzazione di un impianto combinato: un caso studio
Puoi scaricare gratuitamente questo appunto in versione integrale.